- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 1299
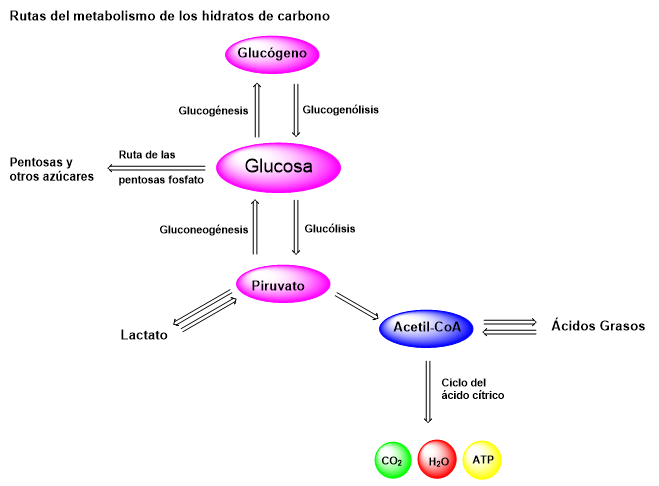 Las células están constantemente activas, dependiendo de una serie de reacciones bioquímicas complejas y coordinadas para subsistir. En esta sección detallaremos las rutas clave en el metabolismo de los carbohidratos en animales. Una de estas, la glucólisis, una vía metabólica primitiva presente en la mayoría de los seres vivos, permite la conversión de glucosa en dos moléculas de piruvato, capturando una pequeña cantidad de energía. Además, se explica la síntesis y descomposición del glucógeno (una reserva de glucosa en vertebrados) a través de la glucogénesis y glucogenólisis, respectivamente, dependiendo de los niveles de glucosa. Otro proceso, la gluconeogénesis, fabrica glucosa a partir de fuentes no carbohidratadas. La vía de las pentosas fosfato transforma la glucosa-6-fosfato en ribosa-5-fosfato (necesaria para la síntesis de nucleótidos y ácidos nucleicos) y otros monosacáridos, produciendo también NADPH, esencial como agente reductor en la célula. También trataremos rutas adicionales en secciones posteriores, incluyendo la fotosíntesis, que usa la energía lumínica para sintetizar carbohidratos, y el ciclo del glioxilato, a través del cual algunos organismos, principalmente plantas, generan carbohidratos a partir de ácidos grasos.
Las células están constantemente activas, dependiendo de una serie de reacciones bioquímicas complejas y coordinadas para subsistir. En esta sección detallaremos las rutas clave en el metabolismo de los carbohidratos en animales. Una de estas, la glucólisis, una vía metabólica primitiva presente en la mayoría de los seres vivos, permite la conversión de glucosa en dos moléculas de piruvato, capturando una pequeña cantidad de energía. Además, se explica la síntesis y descomposición del glucógeno (una reserva de glucosa en vertebrados) a través de la glucogénesis y glucogenólisis, respectivamente, dependiendo de los niveles de glucosa. Otro proceso, la gluconeogénesis, fabrica glucosa a partir de fuentes no carbohidratadas. La vía de las pentosas fosfato transforma la glucosa-6-fosfato en ribosa-5-fosfato (necesaria para la síntesis de nucleótidos y ácidos nucleicos) y otros monosacáridos, produciendo también NADPH, esencial como agente reductor en la célula. También trataremos rutas adicionales en secciones posteriores, incluyendo la fotosíntesis, que usa la energía lumínica para sintetizar carbohidratos, y el ciclo del glioxilato, a través del cual algunos organismos, principalmente plantas, generan carbohidratos a partir de ácidos grasos.
Leer más: Introducción al metabolismo de los hidratos de carbono
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 665
Embárquese en un viaje al corazón de la célula, donde la glucólisis, esa danza molecular ancestral, se desarrolla con elegancia. Imagínese a sí mismo en un mundo microscópico, donde esta serie de transformaciones químicas esencial se despliega, un legado bioquímico compartido por todos los seres vivos, desde las más sencillas bacterias hasta el ser humano.
En este proceso, que bien podría llamarse el ballet de Embden-Meyerhof-Parnas, una simple molécula de glucosa se descompone en dos actores más pequeños, el piruvato, cada uno portando tres átomos de carbono como insignias. A lo largo de este espectáculo, algunos de estos átomos de carbono se someten a una transformación, liberando una modesta pero vital cantidad de energía, apenas un 5% del potencial total, capturada en las formas elegantes de ATP y NADH.
Imagine que el destino del piruvato es una encrucijada, determinada por el ambiente en el que reside la célula. En los dominios sin oxígeno, el piruvato se transforma en una variedad de productos, como el etanol o el ácido láctico, verdaderos testimonios de la vida en condiciones anaeróbicas. Por el contrario, en un escenario oxigenado, el piruvato se somete a una metamorfosis completa, oxidándose hasta convertirse en CO2 y H2O a través de un proceso más complejo conocido como respiración aerobia.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 828
Al adentrarse en el dominio celular, la glucosa, junto con otras formas de azúcares, experimenta un proceso de transformación esencial conocido como fosforilación. Este mecanismo vital bloquea la salida de glucosa de la célula y amplifica la reactividad del oxígeno en el compuesto fosfato creado. Las hexoquinasas, un conjunto de enzimas cruciales, son las encargadas de añadir un grupo fosfato a las hexosas, un proceso que se lleva a cabo en todas las células del cuerpo. Durante esta reacción, el ATP, en colaboración con el Mg2+, forma un complejo esencial, un fenómeno común en las reacciones que involucran quinasas. Esta transformación se caracteriza por su irreversibilidad dentro del ambiente celular, lo que significa que la enzima no puede revertir el producto final a su estado original, sin importar la cantidad de G-6-P presente.
El hígado, un órgano vital en los animales, alberga cuatro variantes de hexoquinasas. Tres de estas enzimas, que se distribuyen en distintos tejidos, muestran una predilección notable por la glucosa, incluso a niveles bajos de concentración en la sangre, asegurando así que tejidos críticos como el cerebro y el músculo puedan acceder a la glucosa necesaria. Estas enzimas regulan su actividad mediante la inhibición por glucosa-6-fosfato, el producto de su propia reacción, evitando la fosforilación excesiva de la glucosa cuando no es necesaria.
La cuarta enzima, conocida como hexoquinasa D o glucoquinasa, desempeña una función distinta, permitiendo que el hígado procese la glucosa para almacenarla como glucógeno. Esta enzima, que opera bajo un conjunto diferente de propiedades cinéticas, se activa con niveles más altos de glucosa y no se ve inhibida por la glucosa-6-fosfato. Esto permite que el hígado comience a almacenar glucosa solo después de que los demás tejidos hayan satisfecho sus necesidades energéticas, regulando de esta manera los niveles de glucosa en la sangre tras la ingesta de alimentos.
Además, entre comidas, cuando los niveles de glucosa en la sangre disminuyen, la glucosa-6-fosfatasa, una enzima exclusiva del hígado (y del riñón bajo ciertas condiciones), juega un papel crucial al liberar glucosa de los almacenes de glucógeno hacia la sangre, garantizando así un suministro constante de energía. Este equilibrio cuidadosamente orquestado subraya la sofisticación del metabolismo celular y la importancia de la regulación enzimática en el mantenimiento de la homeostasis glucémica.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 895
En el segundo acto de la elegante danza de la glucólisis, la molécula de glucosa-6-fosfato se transforma en fructosa-6-fosfato. Esta isomerización es orquestada por la enzima fosfoglucosa isomerasa (PGI), transformando la estructura de aldosa de la glucosa-6-fosfato en la de cetosa de la fructosa-6-fosfato. Esta reacción es reversible, permitiendo que la molécula fluya entre dos formas según las necesidades del momento.
La magia de esta transformación radica en la creación de un intermediario enediol, un estado transitorio que facilita la reorganización de los átomos dentro de la molécula. Este paso no solo es fundamental por la transfiguración que sufre la molécula de glucosa, sino también porque prepara el escenario para la siguiente fase de la glucólisis, haciendo que el carbono en posición 1 de la fructosa resultante esté listo para recibir otro grupo fosfato.
Esta conversión es un ejemplo perfecto de cómo la naturaleza utiliza procesos elegantes y eficientes para preparar las moléculas para reacciones subsecuentes, asegurando así una extracción de energía óptima de cada molécula de glucosa que entra en la célula. En este punto, la glucólisis apenas comienza a revelar su complejidad, preparando el escenario para las intrigas bioquímicas que se desarrollarán en los pasos siguientes.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 1116
La fosfofructoquinasa-1 (PFK-1) lleva a cabo un papel crucial en la glucólisis al añadir un segundo grupo fosfato a la molécula de fructosa-6-fosfato, transformándola en fructosa-1,6-bisfosfato mediante una reacción que no se puede revertir. Este proceso consume una molécula de ATP, lo que resulta en una significativa disminución de la energía libre y marca un compromiso irreversible con la vía glucolítica. La creación de fructosa-1,6-bisfosfato es fundamental, ya que no solo impulsa la célula hacia la glucólisis sino que también previene la pérdida de intermediarios glucolíticos fuera de la célula al dividirse posteriormente en dos triosas fosfato.
PFK-1 actúa como una enzima reguladora clave en este camino metabólico, siendo su actividad finamente controlada por varios factores. Se inhibe en presencia de altas concentraciones de ATP y citrato, señales que indican una alta reserva energética celular y una ralentización del ciclo del ácido cítrico. Por otro lado, el AMP, que se acumula cuando la energía celular es baja, activa a PFK-1, sirviendo como un indicador más fiable de la necesidad energética celular que el ADP. Además, la fructosa-2,6-bisfosfato, generada por la acción de la fosfofructoquinasa-2 (PFK-2) en respuesta a señales hormonales ligadas a los niveles de glucosa en la sangre, potencia la actividad de PFK-1 en el hígado, estimulando la glucólisis y suprimiendo la gluconeogénesis al inhibir la enzima opuesta, fructosa-1,6-bisfosfatasa.
PFK-2, con su doble función, alterna entre actuar como quinasa y fosfatasa en respuesta a las fluctuaciones de los niveles de glucosa sanguínea, reguladas por la insulina y el glucagón. Este mecanismo de regulación refleja la complejidad del control metabólico, asegurando que la glucólisis y la gluconeogénesis se ajusten de manera óptima a las necesidades energéticas de la célula y al estado nutricional del organismo.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 737
La conclusión de la primera fase de la glucólisis se marca por el desdoblamiento de la fructosa-1,6-bisfosfato en dos componentes más pequeños de tres carbonos cada uno: el gliceraldehído-3-fosfato (G-3-P) y la dihidroxiacetona fosfato (DHAP). Esta división es facilitada por una reacción conocida como escisión aldólica, llevada a cabo por la enzima aldolasa. Las reacciones aldólicas, que descomponen las moléculas en un aldehído y una cetona, funcionan en sentido contrario a las condensaciones aldólicas previamente mencionadas.
A pesar de que la energía libre de esta reacción es positiva (+23.8 kJ/mol), indicando que no es espontánea bajo condiciones estándar, el proceso se completa eficientemente en la célula. Esto se debe a la rápida eliminación de los productos de la reacción, lo que permite que el desdoblamiento de la fructosa-1,6-bisfosfato proceda sin impedimentos, avanzando así el camino hacia la extracción de energía de la glucosa.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 877
En este momento de la glucólisis, los dos productos generados por la aldolasa, el gliceraldehído-3-fosfato (G-3-P) y la dihidroxiacetona fosfato (DHAP), entran en una fase de transformación mutua. De estos, solo el G-3-P avanza directamente en la secuencia de reacciones de la glucólisis. Para maximizar la eficiencia del proceso y asegurar que no haya desperdicio de recursos, la dihidroxiacetona fosfato se convierte en gliceraldehído-3-fosfato a través de una reacción de isomerización.
Esta etapa crucial asegura que cada molécula de glucosa introducida en la glucólisis se divide y reforma completamente en dos moléculas de G-3-P, preparando el escenario para la continuación eficiente del desglose glucolítico y la producción energética.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 811
En el paso sexto de la glucólisis, el gliceraldehído-3-fosfato (G-3-P) sufre un proceso de oxidación y fosforilación simultáneas. El resultado de esta reacción es la formación de glicerato-1,3-bisfosfato, una molécula que alberga un enlace rico en energía destinado a la producción de ATP en pasos subsiguientes:
La orquestación de este proceso recae en la gliceraldehído-3-fosfato deshidrogenasa, una enzima compuesta por cuatro subunidades idénticas, cada una equipada con sitios específicos para unir el G-3-P y el NAD+. En un movimiento elegante de bioquímica, la enzima forma un enlace covalente tioéster con el sustrato, facilitando la transferencia de un ion hidruro al NAD+ en el sitio activo. Este intercambio permite que el NADH se retire, dando paso a un nuevo NAD+. Posteriormente, el complejo acil-enzima es asaltado por un fosfato inorgánico, liberando el producto final del sitio activo y avanzando la glucólisis hacia su próxima fase de generación de energía.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 619
En este paso de la glucólisis, la energía se recupera a través de la síntesis de ATP. La fosfoglicerato quinasa actúa como catalizador en la transferencia de un grupo fosforilo de alta energía desde el glicerato-1,3-bisfosfato hacia el ADP, generando ATP:
Este proceso es un claro ejemplo de fosforilación a nivel de sustrato, un mecanismo mediante el cual se sintetiza ATP aprovechando la energía liberada por la transferencia de un grupo fosforilo de un sustrato con alto potencial de transferencia energética. Dado que cada molécula de glucosa se divide para formar dos moléculas de glicerato-1,3-bisfosfato, se producen dos moléculas de ATP por cada glucosa que entra en la ruta, compensando así la inversión energética inicial requerida para añadir grupos fosfato a la glucosa al comienzo de la glucólisis. Este paso no solo equilibra la balanza energética sino que también establece las bases para cualquier ganancia neta de ATP a lo largo del proceso.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 552
La octava etapa de la glucólisis implica la transformación del 3-fosfoglicerato a 2-fosfoglicerato. Dado que el 3-fosfoglicerato presenta un bajo potencial para la transferencia de fosforilo, no es adecuado para la generación de ATP en etapas posteriores. Para superar esto, las células lo convierten en fosfoenolpiruvato (PEP), un compuesto con un potencial de transferencia de fosforilo significativamente más alto, lo que lo hace un candidato ideal para la síntesis de ATP. La diferencia en las energías libres estándar de hidrólisis entre el 3-fosfoglicerato (-12.6 kJ/mol) y el PEP (-58.6 kJ/mol) subraya la importancia de esta transformación. En el inicio de este proceso, una enzima llamada fosfoglicerato mutasa facilita el cambio de la posición del grupo fosforilo del carbono 3 al carbono 2, empleando un mecanismo de dos pasos de adición y eliminación.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 609
La novena fase de la glucólisis implica la transformación del 2-fosfoglicerato en fosfoenolpiruvato (PEP) a través de un proceso de deshidratación llevado a cabo por la enzima enolasa:
El PEP destaca por su elevado potencial de transferencia de grupo fosforilo, superior al del 2-fosfoglicerato, debido a la presencia de un grupo enol-fosfato en vez de un simple éster fosfato. Este incremento en el potencial se comprende mejor al observar la siguiente reacción. Aldehídos y cetonas pueden existir en dos formas isoméricas; la forma enol, que presenta un doble enlace carbono-carbono junto a un grupo hidroxilo, y la forma ceto, más estable, que incluye un grupo carbonilo. La conversión entre estas dos formas, conocidas como tautómeros, se denomina tautomerización.
La tautomerización se ve limitada por la presencia del grupo fosfato, al igual que la estabilización por resonancia del ion fosfato libre. Por tanto, en esta etapa de la glucólisis, la transferencia de fosforilo al ADP se ve altamente favorecida, preparando el escenario para una eficiente síntesis de ATP en los pasos subsiguientes.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 671
En el acto final de la glucólisis, la enzima piruvato quinasa juega el papel estelar al transferir un grupo fosforilo del PEP al ADP, culminando en la creación de dos moléculas de ATP a partir de cada molécula de glucosa procesada.
El gran potencial energético de hidrólisis del PEP impulsa su transformación en piruvato de manera irreversible. Esta considerable liberación de energía libre, que caracteriza la irreversibilidad de la reacción, está ligada a la tautomerización espontánea del piruvato desde su forma enol, menos estable, a la forma ceto, su configuración más estable y energéticamente favorable.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 2675
El camino del piruvato tras la glucólisis desemboca en dos potenciales destinos, dependiendo de la presencia de oxígeno. Durante la glucólisis, cada molécula de glucosa se descompone para generar un balance energético de dos ATP y dos NADH. El piruvato, cargado de energía, tiene el potencial de continuar este rendimiento energético, pero necesita transformarse en acetil-CoA mediante un proceso de descarboxilación para adentrarse en el ciclo del ácido cítrico. Este ciclo, también conocido como ciclo de Krebs, es una central metabólica que oxida los átomos de carbono del acetil-CoA a CO2, generando NADH en el proceso.
Con oxígeno disponible, el NADH entra en el sistema de transporte electrónico, donde sus electrones se transfieren a través de una cadena de reacciones de oxidación-reducción hasta alcanzar el oxígeno, formando agua. Este flujo electrónico está intrínsecamente ligado a la creación de un gradiente de protones que facilita la síntesis de ATP, destacando la eficiencia de la respiración celular aeróbica.
En ambientes sin oxígeno, la situación es distinta. La oxidación adicional del piruvato se ve bloqueada, y diferentes células adoptan estrategias para regenerar el NAD+ necesario para mantener activa la glucólisis. Este mecanismo de salvaguarda se conoce como fermentación. En este contexto, el piruvato se convierte en lactato en células musculares y algunas bacterias, como el Lactobacillus, para producir NAD+ y permitir que la glucólisis prosiga. Este entramado de reacciones bioquímicas subraya la flexibilidad y adaptabilidad del metabolismo celular ante condiciones cambiantes.
Los microbios que generan energía a través de la fermentación láctica se clasifican en dos categorías principales. Los primeros son los fermentadores homolácticos, especialistas en la producción exclusiva de lactato, un ejemplo típico lo constituyen diversas bacterias lácticas que son esenciales en la industria láctea. Por otro lado, los fermentadores heterolácticos o mixtos diversifican su producción, generando una gama de ácidos orgánicos. Un escenario donde esto es evidente es en el rumen del ganado, donde microorganismos simbióticos, capaces de descomponer celulosa, producen una mezcla de ácidos orgánicos como el láctico, acético, propiónico, y butírico, que el ganado absorbe como nutrientes. Además, estos procesos fermentativos liberan gases como el metano y dióxido de carbono.
Por otro lado, la fermentación alcohólica es el dominio de las levaduras y algunas especies bacterianas. Las levaduras transforman el piruvato en acetaldehído, que luego se reduce a etanol en presencia de NADH. Este proceso, aparte de ser un fenómeno biológico fascinante, tiene aplicaciones prácticas significativas en la producción de bebidas alcohólicas como el vino y la cerveza, así como en la panificación. Además, ciertas bacterias, tales como Clostridium acetobutylicum – pariente cercano de los organismos causantes del botulismo y el tétanos – optan por producir butanol en lugar de etanol. Aunque tradicionalmente este microorganismo fue utilizado en la síntesis comercial de butanol para la producción de detergentes y fibras sintéticas, los avances en la síntesis química basada en petróleo han relegado este método biológico a un segundo plano.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 1345
La glucólisis, un proceso fundamental en la bioquímica celular, implica la degradación de la glucosa hasta formar piruvato, liberando energía aprovechable por la célula. Aunque a primera vista el proceso parece directo, con una producción neta de dos moléculas de ATP por cada molécula de glucosa descompuesta, un análisis más detenido de la energética de la glucólisis revela una complejidad subyacente que es esencial para entender cómo las células extraen energía de manera eficiente.
Para comprender la eficacia energética de la glucólisis, es crucial examinar no solo las reacciones individuales y su energía libre estándar, sino también el contexto celular en el que estas reacciones ocurren. Las condiciones intracelulares, como el pH y las concentraciones de metabolitos, juegan un papel determinante en la dinámica energética de la glucólisis. Un estudio de las variaciones de energía libre bajo estas condiciones reales, especialmente en los eritrocitos, revela patrones fascinantes.
Dentro de las diez reacciones que componen la glucólisis, tres específicamente —las catalizadas por la hexoquinasa, la fosfofructoquinasa-1 (PFK-1), y la piruvato quinasa— presentan valores de cambio de energía libre () significativamente negativos en el ambiente celular. Estas reacciones son prácticamente irreversibles en el sentido de que se completan una vez iniciadas, marcando etapas clave de control en la ruta glucolítica. La irreversibilidad de estas reacciones asegura que la glucólisis proceda en una dirección determinada, canalizando eficientemente la glucosa hacia la producción de energía y precursores metabólicos.
Las reacciones restantes de la glucólisis, identificadas con valores de cercanos a cero, se hallan en un equilibrio más dinámico. Esta característica les permite ser reversibles, adaptando su dirección en respuesta a cambios sutiles en las concentraciones de sustratos y productos. Esta reversibilidad es crucial para la regulación metabólica y permite que la vía de la glucólisis se ajuste rápidamente a las necesidades energéticas de la célula.
Es interesante notar que la gluconeogénesis, el proceso metabólico que sintetiza glucosa a partir del piruvato y otros compuestos, evita precisamente las etapas irreversibles de la glucólisis. En lugar de utilizar las mismas enzimas para los pasos 1, 3, y 10, la gluconeogénesis emplea enzimas distintas, permitiendo así la síntesis de glucosa incluso cuando la demanda energética de la célula cambia.
La estrategia de utilizar reacciones irreversibles para dirigir y controlar el flujo metabólico es un principio clave en la bioenergética celular. Permite a las células maximizar la eficiencia de la glucólisis, asegurando que la energía y los precursores metabólicos estén disponibles cuando se necesiten. Este equilibrio cuidadosamente regulado entre las reacciones reversibles e irreversibles dentro de la glucólisis subraya la sofisticación de los sistemas biológicos en la gestión de la energía vital para la vida celular.
- Detalles
- Escrito por: Germán Fernández
- Categoría: Metabolismo de los hidratos de carbono
- Visitas: 5020
La glucólisis, esencial para la vida celular, convierte la glucosa en piruvato, generando energía (ATP) y precursores metabólicos. Este proceso no solo es vital para la producción energética sino que también juega un rol importante en la síntesis de numerosos metabolitos. Dada su importancia, la regulación de la glucólisis es sumamente compleja y finamente ajustada.
El control de la velocidad de la glucólisis se ejerce principalmente a través de la regulación alostérica de tres enzimas críticas: la hexoquinasa, la fosfofructoquinasa-1 (PFK-1) y la piruvato quinasa. Estas enzimas catalizan reacciones esencialmente irreversibles, actuando como guardianes que regulan el flujo de glucosa a través de esta vía metabólica.
Los reguladores alostéricos, que son moléculas cuyas concentraciones reflejan el estado metabólico celular, juegan un papel central en este mecanismo de control. Estos efectores pueden activar o inhibir las enzimas clave, ajustando así la tasa de glucólisis según las necesidades energéticas y metabólicas de la célula.
Por ejemplo, la hexoquinasa, que inicia el proceso glucolítico, se inhibe por su producto, la glucosa-6-fosfato. Esta retroalimentación negativa previene la acumulación innecesaria de intermediarios glucolíticos cuando la célula tiene suficiente glucosa.
Además, la presencia de AMP, que señaliza bajos niveles de energía celular, activa la PFK-1 y la piruvato quinasa, estimulando la glucólisis para generar ATP. En contraste, altas concentraciones de ATP indican que la célula tiene suficiente energía, lo que resulta en la inhibición de estas enzimas y, por lo tanto, en una desaceleración de la glucólisis.
Otros metabolitos como el citrato y la acetil-CoA, que se acumulan durante períodos de abundancia energética, inhiben la PFK-1 y la piruvato quinasa respectivamente, ejerciendo un control adicional sobre la glucólisis.
Un mecanismo interesante de regulación es el papel de la fructosa-2,6-bisfosfato, que activa la PFK-1. Esta molécula es producida en respuesta a señales hormonales que indican altas concentraciones de glucosa en la sangre, promoviendo así la glucólisis cuando hay glucosa disponible. Además, la acumulación de fructosa-1,6-bisfosfato actúa como un activador alostérico de la piruvato quinasa, proporcionando un mecanismo de retroalimentación positiva que asegura la continuación eficiente de la glucólisis una vez iniciada.
Este delicado equilibrio de activadores e inhibidores asegura que la glucólisis se ajuste dinámicamente a las condiciones celulares, optimizando la generación de energía y la síntesis de metabolitos necesarios para el crecimiento y la supervivencia celular. La capacidad de la célula para regular finamente este proceso metabólico fundamental destaca la complejidad y la eficiencia de los sistemas biológicos.
¿Qué es la regulación alostérica?
La regulación alostérica es un mecanismo de control enzimático que modifica la actividad de una enzima mediante la unión de una molécula reguladora (efector alostérico) en un sitio específico de la enzima, distinto del sitio activo donde se unen los sustratos. Este sitio específico se conoce como sitio alostérico. La unión del efector alostérico induce un cambio conformacional en la estructura terciaria o cuaternaria de la enzima, lo que puede aumentar (activación alostérica) o disminuir (inhibición alostérica) su actividad catalítica.
La regulación alostérica permite a las células ajustar finamente las velocidades de las reacciones metabólicas en respuesta a cambios en el ambiente interno o externo, lo que facilita la homeostasis y la respuesta a condiciones metabólicas cambiantes. Los efectores alostéricos pueden ser productos finales de una vía metabólica (feedback negativo o retroalimentación negativa), precursores, metabolitos intermediarios, iones o incluso otras proteínas o moléculas señalizadoras.
Este tipo de regulación es fundamental en vías metabólicas críticas, como la glucólisis y la síntesis de ácidos nucleicos y proteínas, ya que permite una respuesta coordinada y adaptativa de la célula a sus necesidades energéticas y constructivas. La regulación alostérica asegura que las rutas metabólicas sean eficientes y se activen o desactiven según sea necesario, evitando la sobreproducción o escasez de compuestos esenciales.

